Sanidad alerta de la "interacción potencialmente mortal" al mezclar estos dos medicamentos
Se tratan de fármacos para combatir el herpes zóster y el cáncer
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), dependiente del Ministerio de Sanidad, ha hecho una advertencia sobre los "riesgos potencialmente mortales" que tiene la administración conjunta de dos fármacos empleados para combatir el herpes zóster y el cáncer. Concretamente se refiere a la interacción de Brivudina (Nervinex y Brivudina Aristo) con antineoplásicos que contienen 5-fluoropirimidinas (capecitabina, 5-fluorouracilo, tegafur, floxuridina) y con fluocitosina
La Brivudina es un análogo de nucleósidos inhibidor de la replicación del virus varicela-zoster, indicado en el tratamiento precoz del herpes zoster agudo en adultos inmunocompetentes. Actualmente en España están autorizados dos medicamentos que contienen este principio activo: Nervinex y Brivudina Aristo.
Brivudina, a través de su principal metabolito bromovinil uracilo, ejerce una inhibición irreversible de la dihidropirimidina deshidrogenasa, una enzima que regula el metabolismo tanto de los nucleósidos naturales (por ejemplo, timidina) como de medicamentos tipo pirimidina (fluoropirimidinas) tales como capecitabina o 5-fluorouracilo (5-FU). Como consecuencia de la inhibición enzimática, se produce una sobreexposición y un aumento de la toxicidad de las fluoropirimidinas potencialmente mortal.
Por tanto, la administración concomitante de brivudina y fluoropirimidinas está contraindicada y estas no pueden administrarse durante el tratamiento con brivudina, ni en las cuatro semanas posteriores a la finalización del mismo
A pesar de la estrategia informativa realizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) acerca de esta contraindicación de consecuencias potencialmente mortales para el paciente, el Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano (SEFV-H) sigue recibiendo notificaciones de casos debidos a la administración conjunta de brivudina y antineoplásicos que contienen 5-fluoropirimidinas. En concreto, desde 2017 se han notificado seis nuevos casos de esta interacción, todos graves y cuatro de ellos con desenlace mortal.
Teniendo en cuenta los datos expuestos anteriormente, la AEMPS considera necesario recordar:
Información para profesionales sanitarios
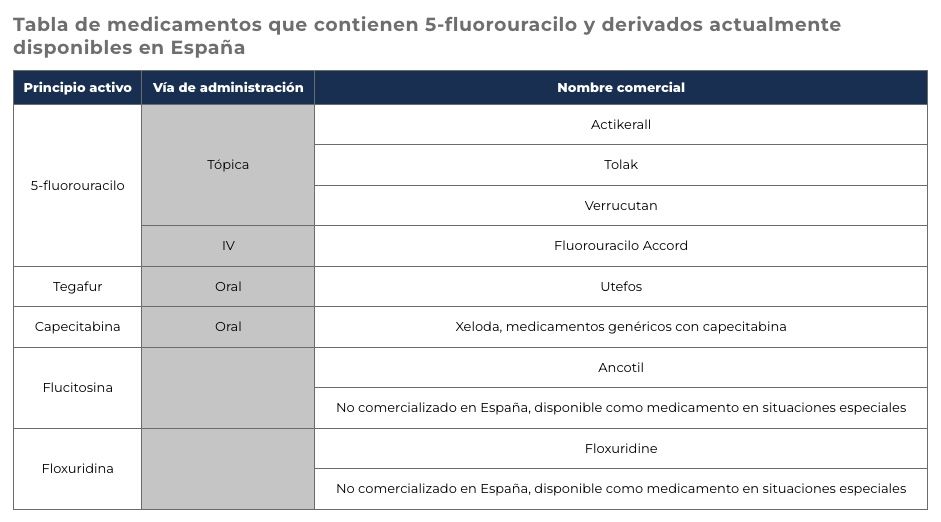
- Antes de prescribir brivudina es indispensable asegurarse de que el paciente no está recibiendo quimioterapia antineoplásica ni ninguna preparación tópica que contenga 5-fluoropirimidinas (ver la tabla inferior con los medicamentos implicados).
- No debe administrarse brivudina (Nervinex y Brivudina Aristo) a pacientes que recientemente han recibido o estén recibiendo quimioterapia antineoplásica con medicamentos que contienen 5-fluorouracilo (5-FU), incluyendo también sus preparaciones tópicas, sus profármacos (por ejemplo, capecitabina, tegafur), combinación de fármacos que contengan estos principios activos u otras fluoropirimidinas o tratamiento antifúngico con flucitosina.
- No comenzar tratamiento con los medicamentos mencionados en el punto anterior en pacientes que hayan finalizado el tratamiento con brivudina en el último mes (es necesario esperar al menos 4 semanas desde la finalización del tratamiento con brivudina).
- En caso de administración accidental de brivudina a pacientes que recientemente han recibido o están recibiendo fluoropirimidinas, es preciso suspender la administración de ambos fármacos y tomar las medidas adecuadas para reducir la toxicidad de las fluoropirimidinas. Se recomienda hospitalización inmediata y medidas para prevenir infecciones sistémicas y la deshidratación. Los síntomas de toxicidad por fármacos fluoropirimidínicos se manifiestan con náuseas, vómitos, diarrea y, en casos graves, estomatitis, mucositis, necrólisis epidérmica tóxica, neutropenia y depresión de la médula ósea.
- En el momento de la dispensación de brivudina, es necesario informar y recordar al paciente que lea las advertencias del envase, la tarjeta de información incluida en el mismo y el prospecto del medicamento.
Información para pacientes
- Para prevenir reacciones adversas que pueden ser graves, antes de comenzar a tomar Nervinex o Brivudina Aristo, medicamentos para el tratamiento del herpes zoster, lea la tarjeta de información para el paciente incluida en el envase y el prospecto del medicamento. Consulte cualquier duda con el profesional médico o farmacéutico.
- No tome los medicamentos Nervinex ni Brivudina Aristo si está recibiendo algún medicamento para el tratamiento del cáncer o el medicamento Ancotil para una infección por hongos, debiendo evitarlo durante todo el tiempo de tratamiento.
- Si ha tomado Nervinex o Brivudina Aristo debe esperar un mínimo de 4 semanas antes de recibir un tratamiento para el cáncer con cualquier medicamento mencionado en la tabla de más abajo.
- Si por error ha tomado brivudina y uno de los medicamentos de la tabla inferior, interrumpa la toma de ambos medicamentos y acuda a un hospital para recibir tratamiento inmediato.