Hito en los xenotrasplantes: un hombre vive 38 días con un hígado de cerdo modificado
Beatriz Domínguez-Gil (ONT): "Esto demuestra que los xenotrasplantes ya no son ciencia ficción"
El mundo de los xenotrasplantes avanza a pasos de gigante. Un importante estudio publicado en el Journal of Hepatology acaba de informar sobre el primer xenotrasplante hepático auxiliar del mundo de un cerdo genéticamente modificado a un receptor humano vivo. El paciente sobrevivió 171 días –38 con el injerto de cerdo, que hubo que retirar–, lo que demuestra que los hígados porcinos modificados genéticamente pueden contribuir a funciones metabólicas y sintéticas clave en humanos, a la vez que pone de relieve las complicaciones que actualmente limitan los resultados a largo plazo.
Según datos del Observatorio Global de Donación y Trasplante, que gestiona la Organización Nacional de Trasplantes (ONT), como centro colaborador de la Organización Mundial de la Salud (OMS), en 2024 se realizaron 42.495 trasplantes hepáticos en el mundo. En Europa (datos de 40 países miembros del Consejo de Europa), fueron 11.019 los trasplantes hepáticos realizados, cifra que contrasta con los 22.215 pacientes en lista de espera, de los que 2.314 fallecieron antes de ser trasplantados.
En declaraciones a 65YMÁS, Beatriz Domínguez-Gil, directora de la ONT, aclara: "Efectivamente este es un hito médico que constata la rápida evolución del xenotrasplante. Pero debemos insistir en su carácter experimental y en los muchos obstáculos que quedan por resolver. Es necesario refinar las modificaciones genéticas efectuadas en los animales, mejorar la inmunosupresión y tratar de identificar y gestionar de manera temprana complicaciones graves, como la desarrollada por este paciente, que finalmente falleció.
El caso
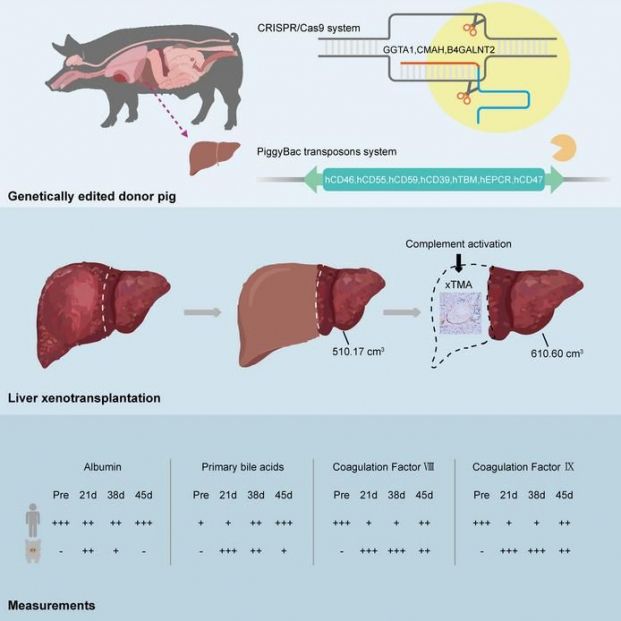
Es Beicheng Sun, presidente del primer hospital afiliado a la Universidad Médica de Anhui (Chima) y miembro del equipo que ha llevado a cabo este primer xenoinjerto en receptor vivo, quien nos las aclara: “El caso se refería a un hombre de 71 años con cirrosis relacionada con la hepatitis B y carcinoma hepatocelular, que no era apto para resección ni trasplante de hígado humano. Implantamos un injerto auxiliar de un cerdo miniatura Diannan modificado genéticamente con 10 modificaciones genéticas, incluyendo genes knockout de xenoantígenos y transgenes humanos para mejorar la compatibilidad inmunitaria y de coagulación”.
Y señala: “Durante el primer mes tras la cirugía, el injerto funcionó eficazmente, produciendo bilis y sintetizando factores de coagulación, sin evidencia de rechazo agudo ni hiperagudo. Sin embargo, el día 38, el injerto se retiró tras el desarrollo de una microangiopatía trombótica asociada al xenotrasplante (xMAT), una complicación grave relacionada con la activación del complemento y la lesión endotelial. El tratamiento con el inhibidor del complemento eculizumab y la plasmaféresis resolvieron con éxito la xMAT. A pesar de ello, el paciente sufrió posteriormente episodios repetidos de hemorragia gastrointestinal superior y falleció el día 171”.
Insiste el experto en que “durante el primer mes después de la cirugía, el paciente se recuperó muy bien. Sin embargo, después de un mes, se presentó la MAT y fue difícil tomar la decisión de retirar el xenoinjerto. Se realizó tratamiento para la MAT y terapia endoscópica para la hemorragia gástrica superior”.
El Dr. Sun sentencia que la causa por la que falleció el paciente fue de “hemorragias recurrentes por varices gástricas debido a cirrosis hepática”. Pero adelanta: “Estoy trabajando en un cerdo de nueva generación modificado genéticamente. Contamos con un cerdo modificado genéticamente de 12 genes que se probará en un paciente fallecido.
Mirando hacia atrás es importante recordar que durante décadas, el xenotrasplante se ha considerado una posible solución a la escasez de órganos. “Lo que estamos viendo ahora, con trabajos como este, es que esto no es ciencia ficción, sino que estamos más cerca de un futuro donde los xenotrasplantes puedan ser una realidad para pacientes en lista de espera. En EE.UU ya se están llevando a cabo ensayos clínicos de xenotrasplantes en pacientes seleccionados, aprobados por la FDA. En Europa se va con más retraso, si bien tenemos un equipo bien preparado para participar en estos estudios, el liderado por el De. Pablo Ramírez”, declara la directora de la ONT.
En España
Fue hace 25 años cuando se obró el milagro en Murcia. .Cirujanos del Hospital Virgen de la Arrixaca trasplantaron un hígado de cerdo en un babuino y este sobrevivió más de una semana con él. Pablo Ramírez es jefe del servicio de cirugía general y del aparato digestivo del hospital murciano, y es, además, uno de los principales impulsores de los xenotrasplantes en Europa y forma parte del comité que ha establecido el Consejo de Europa para la evaluación ética y regulatoria de este tipo de intervenciones.
Los otros hítos históricos: corazón y riñón
En los últimos tres años se han reportado xenotrasplantes exitosos de corazón en un hombre de 57 años cuyo caso se recogió el 22 de junio de 2022 en el New England Journal of Medicne y el de riñón. Publicado en la misma revista el 7 de ferebro de 2025 se trató de un varón de 62 años.
Los desafíos del hígado
Sin embargo, desde hace tiempo se ha considerado que los desafíos que plantea el hígado son distintos a los del corazón o el riñón. Mientras que las barreras inmunológicas predominan en el trasplante de riñón y corazón, el hígado plantea problemas adicionales y complejos de incompatibilidad fisiológica, que abarcan múltiples sistemas enzimáticos, funciones sintéticas y actividad reticuloendotelial.
Los importantes avances en la transferencia nuclear de células somáticas han ayudado a superar la incompatibilidad entre especies, una barrera clave para el xenotrasplante, y han conducido a la reciente aprobación por parte de la FDA de cerdos modificados genéticamente bajo una Solicitud de Nuevo Medicamento Animal, abriendo así la puerta al uso de órganos de cerdo como donantes adecuados para humanos.
Estas complejas modificaciones genéticas del órgano donante porcino tienen como objetivo evitar el rechazo agudo hiperinmune (principalmente mediante la inactivación del gen porcino que codifica la alfa-1,3-galactosiltransferasa), prevenir complicaciones vasculares y facilitar la compatibilidad del xenoinjerto (principalmente mediante la inserción de transgenes humanos que inhiben la cascada del complemento, la coagulación y la inflamación.
A pesar de ello, los modelos preclínicos de trasplante hepático de cerdo a primate han demostrado una supervivencia medida en días o semanas, como se documenta en un trabajo de American Journal of Trasplant, mucho menor que la alcanzada en el trasplante xenogénico de corazón o riñón.
El próximo año
En consecuencia, la mayoría de los investigadores han considerado el xenohígado menos como un órgano de destino y más como un puente temporal: hacia la recuperación en la insuficiencia hepática aguda (IAA) o en casos de "pequeño para el tamaño" tras una resección mayor, o hacia el trasplante "convencional" en la insuficiencia hepática aguda sobre crónica (IAAC). El primer ensayo para evaluar si hígados de cerdo modificados genéticamente conectados durante 72 h como soporte hepático extracorpóreo pueden beneficiar a los pacientes con ACLF está previsto que comience a finales de 2025, como se anuncia en Nature
Sin embargo, el xenotrasplante hepático auténtico seguía siendo difícil de alcanzar hasta el reciente informe del equipo de Tao sobre un procedimiento auxiliar heterotópico en un receptor con muerte cerebral recogido también en la revista anterior.
Prueba previa a la publicación
El hígado de cerdo, con seis genes editados, comenzó a funcionar en 2 horas sin inducir rechazo durante los 10 días siguientes (a costa de un régimen inmunosupresor intensivo de ocho fármacos). Demostró una función sintética y una adaptación hemodinámica aceptables, pero una reserva funcional limitada, como lo indican los niveles persistentemente altos de bilirrubina.

Beatriz Domínguez-Gil, directora de la ONT
"El informe de Zhang en este número de la revista Journal of Hepatology marca un gran avance en la viabilidad del xenotrasplante hepático. El caso, como se ha dicho anteriormente, se refiere a un hombre de 71 años con cirrosis relacionada con el Viruis de la Hepatits B y un carcinoma hepatocelular de gran tamaño, en quien se preveía que la resección del tumor dejaría un hígado remanente insuficiente. Por razones humanitarias, se implantó un injerto auxiliar de hígado de cerdo ortotópico. Técnicamente, la operación fue un éxito. El injerto funcionó, produjo factores de coagulación —sorprendentemente, en su mayoría de origen porcino— y mantuvo la capacidad de síntesis en la fase postoperatoria temprana. No se produjo rechazo hiperagudo y se emplearon inmunosupresores estándar autorizados, sin recurrir a métodos experimentales”, documenta la directora de la ONT.
Desde un punto de vista funcional, el caso es sorprendente. “El injerto produjo bilis, albúmina y factores de coagulación mensurables en el suero del receptor; la albúmina porcina fue demostrablemente activa (se detectaron albúminas porcina y humana mediante ELISA), y la combinación de albúminas mantuvo una presión oncótica normal. La medición de ácidos biliares y factores de coagulación específicos de los cerdos proporciona una valiosa perspectiva mecanicista sobre el rendimiento metabólico del injerto. Estos datos, en conjunto, muestran que el xenolípido puede asumir funciones hepáticas críticas, al menos transitoriamente”, insiste.
Los autores y sus colaboradores abordaron además el riesgo del retrovirus endógeno porcino (PERV, de sus siglas en inglés): la evidencia actual sugiere que los tres subtipos de PERV (A, B y C) podrían poseer potencial patógeno y que sería preferible la inactivación completa de todos los subtipos
“En este caso, el hígado de cerdo auxiliar se extrajo el día 38 del postoperatorio debido a la xMAT. Finalmente, a pesar de la función temporal, el xenotrasplante no pudo prevenir una hemorragia gastrointestinal mortal, que se produjo 6 meses después”.
La opinión
Como recuerda en un editorial el Dr. Heiner Wedemeyer, coeditor de la revista y del Departamento de Gastroenterología, Hepatología, Enfermedades Infecciosas y Endocrinología de la Facultad de Medicina de Hannover que acompaña al estudio “científicamente, el caso demuestra que un hígado de cerdo modificado genéticamente puede injertarse, funcionar y proporcionar soporte sintético en un receptor humano, al menos durante varias semanas. Clínicamente, sin embargo, el resultado subraya las limitaciones de la tecnología actual, especialmente en lo que respecta a la supervivencia a largo plazo y las complicaciones”.
Desde el punto de vista ético, “el uso de xenotrasplantes en un paciente con cirrosis avanzada generará debate sobre la selección de pacientes y las indicaciones adecuadas. Estratégicamente, el caso podría reavivar el debate sobre si los hígados xenogénicos deberían considerarse como terapias de destino o si su verdadero valor reside en estrategias puente a corto plazo, apoyando a los pacientes con IHA, IHAC o insuficiencia hepática asociada a resección hasta que la recuperación o el alotrasplante sean posibles”, insiste el experto.
“Esta operación aún no abre la puerta al uso clínico generalizado de hígados de cerdo. Pero sí establece una prueba de concepto de que estos injertos pueden funcionar en humanos”, enfatiza Beatriz Domínguez-Gil
“Este caso demuestra que un hígado de cerdo modificado genéticamente puede funcionar en un ser humano durante un período prolongado”, explica. Beicheng Sun. Defiende, además que "es un avance crucial que demuestra tanto las posibilidades como los obstáculos pendientes, en particular los relacionados con la desregulación de la coagulación y las complicaciones inmunitarias, que deben superarse”.
“Este informe es un hito en hepatología. Demuestra que un hígado porcino modificado genéticamente puede injertarse y proporcionar funciones hepáticas clave en un receptor humano. Al mismo tiempo, destaca los desafíos biológicos y éticos que aún persisten antes de que estos enfoques puedan traducirse en un uso clínico más amplio. El xenotrasplante puede abrir caminos completamente nuevos para pacientes con insuficiencia hepática aguda, insuficiencia hepática crónica aguda y carcinoma hepatocelular. Ha comenzado una nueva era en la hepatología de trasplantes, comenta Wedemeyer.
