El dolor crónico dura más en las mujeres por culpa de las hormonas
Las diferencias entre sexos en las células inmunes reguladas hormonalmente son el motivo

Hablar de dolor crónico es documentar que es aquel que dura más de tres meses y que es una de las cinco principales causas subyacentes de años vividos con discapacidad a nivel mundial, según la Asociación Internacional para el Estudio del Dolor.
Las cifras de afectadas y afectados no son nada desdeñables. Según la Sociedad Española de Neurología, más del 30% de la población sufre algún tipo de dolor, principalmente personas entre los 45 y los 54 años de edad y, en un 60% de los casos, mujeres. Pero, además, un 18% de la población padece algún tipo de dolor crónico, es decir, se enfrenta a él desde hace más de 3 meses, y más de un 5% de la población lo sufre diariamente. Ahora, además, acabamos de saber que en el caso de esta dolencia, el ‘sexo sí importa’.
En un nuevo artículo publicado en Science Immunology, investigadores de la Universidad Estatal de Michigan (MSU. EE.UU) han descubierto los motivos por los que el dolor crónico dura más en ellas que en ellos. Como se especifica en Nature Reviews Neuroscience, existe un claro predominio femenino en la mayoría de los síndromes de dolor crónico, probablemente impulsado por una resolución más lenta del dolor en ellas, se documenta en un estudio de Spine.
La testosterona
Esta resolución más lenta del dolor en las mujeres aumenta su riesgo de transición a dolor crónico. Dada la fuerte asociación entre el sistema inmunitario y el dolor, así como las diferencias de género en las respuestas inmunitarias, los mecanismos inmunitarios podrían contribuir a las diferencias de género en el dolor.
Así, la nueva investigación sugiere que las diferencias en las células inmunes reguladas por hormonas, llamadas monocitos, pueden ayudar a explicar por qué. Los investigadores han descubierto que un subconjunto de monocitos libera una molécula para inhibir el dolor. El equipo también ha encontrado que estas células son más activas en los hombres debido a niveles más altos de hormonas sexuales como la testosterona.
En el ensayo, las hembras experimentaron un dolor más prolongado y una recuperación más tardía debido a la menor actividad de sus monocitos. Geoffroy Laumet, profesor asociado de fisiología de la MSU, y Jaewon Sim, ex estudiante de posgrado de su laboratorio, descubrieron el mismo patrón tanto en modelos murinos como en pacientes humanos.
Estos hallazgos, financiados por los Institutos Nacionales de Salud y el Departamento de Defensa estadounidenses, podrían significar que esas células inmunitarias pueden ser manipuladas para producir más señales que calmen el dolor. Si bien es probable que un nuevo tratamiento esté a décadas de distancia, el Dr, Laumet espera que esta investigación pueda algún día ayudar a millones de personas a experimentar alivio con tratamientos sin opioides y garantizar que el dolor de las mujeres se tome en serio.
El dolor en ellas y en ellos
“La diferencia de dolor entre hombres y mujeres tiene una base biológica. No está en la cabeza, ni eres débil. Está en tu sistema inmunitario”, ha declarado Laumet en un comunicado.

Geoffroy Laumet y Sabrina De Souza (Fin Gómez).
El dolor se produce cuando las neuronas de todo el cuerpo se activan mediante estimulación. La mayoría del tiempo permanecen inactivas, pero se activan al golpearse un dedo del pie o caerse de la bicicleta. Sin embargo, en quienes padecen dolor crónico, los sensores pueden activarse con una estimulación leve o incluso sin ninguna estimulación. Los médicos aún confían en que los pacientes califiquen su dolor en una escala del 1 al 10. El problema es que cada persona experimenta el dolor de forma diferente. Por lo tanto, cuando más mujeres que hombres se quejan de dolor prolongado o crónico, la diferencia suele atribuirse a la percepción o a la información.
Laumet ha dedicado su laboratorio al estudio del dolor durante seis años. Su equipo estaba investigando un pequeño proyecto piloto cuando observaron niveles más altos de interleucina-10 (IL-10) en hombres. Cuando la segunda prueba volvió a mostrar niveles más altos de la sustancia que indica a las neuronas que supriman el dolor, se dieron cuenta de que habían descubierto algo.
“Ese fue un punto de inflexión para mí. Me siento muy afortunado de que confiáramos en esos hallazgos iniciales e inciertos y decidiéramos investigarlos más a fondo”, ha explicado Sim.
Una técnica sofisticada
El laboratorio de Laumet se ha adentrado en la investigación mediante una sofisticada técnica llamada citometría de flujo espectral de alta dimensión. Descubrieron que los monocitos, considerados durante mucho tiempo células precursoras sin gran función, desempeñan un papel esencial y directo en la comunicación con las neuronas sensibles al dolor mediante la producción de IL-10. El equipo de Laumet descubrió que los monocitos productores de IL-10 eran mucho más activos en hombres que en mujeres. Al bloquear las hormonas sexuales masculinas, obtuvieron el resultado opuesto.
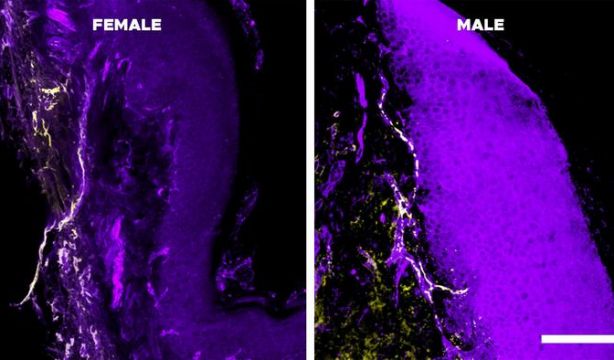
Rreceptor de IL-10, (en amarillo, en células cutáneas femeninas (izqd) y en masculinas (drcha).
“Este estudio demuestra que la resolución del dolor no es un proceso pasivo. Es un proceso activo, impulsado por el sistema inmunitario”, ha aclarado el investigador principal.
Cinco pruebas distintas
El equipo de Laumet ha llevado al menos cinco tipos de pruebas en modelos de ratón para asegurarse de que lo observado no fuera una anomalía. En todas las ocasiones, los resultados fueron los mismos.
Fue entonces cuando contactó con Sarah Linnsteadt, colega de la Universidad de Carolina del Norte en Chapel Hill, quien estudia las consecuencias psicológicas de las personas que sufren accidentes de tráfico. Su investigación ha mostrado un patrón similar: los hombres tenían monocitos productores de IL-10 más activos y el dolor remitía más rápidamente.
Esta nueva evidencia arroja luz sobre la vía inmunoneural de resolución del dolor, cambiando la perspectiva de cómo se origina el mismo a por qué persiste. El siguiente paso es investigar cómo los tratamientos podrían dirigirse a esta vía y estimular la producción de IL-10. Estos tratamientos podrían acelerar la resolución del dolor en lugar de simplemente bloquear las señales de dolor.
“Los futuros investigadores pueden aprovechar este trabajo. Esto abre nuevas vías para terapias sin opioides destinadas a prevenir el dolor crónico antes de que se establezca”, ha puntualizado Laumet.
